课内课外拓展内容-易错&重点&拓展
你好!这里整理了化学学习过程中你可能有过的疑点和课外拓展内容。注重强调从原理层面搞懂,相信一定会或多或少对你有帮助
“高x上/下学期”内的内容不仅局限于该学期所学的教科书,而是我自己在学习时问过/了解的所有内容,已经尽心整理了,因此建议顺序阅读。
在阅读之前… 本文所有内容和资料均为独自搜集,系统化整理耗费巨大精力和心血,请遵守 CC BY-NC-SA 4.0 版权协议。部分内容转自 Wikipedia,以上述协议引用
现在,开始吧!
高一上学期
1、向蛋白质溶液中加入NaCl溶液,出现白色沉淀(盐析);继续加水,沉淀消失
2、存在固体酸,如
3、甲基橙的变色pH范围:
4、两性氧化物:
5、球形冷凝管:减少产品损失/原料浪费(下三图第一)
6、 增重问题:H照单全收,C多则增重多,O多则增重少
- 具体原理:

7、可发生反应:
8、 并非无定形,而是有着六方晶系结构; 为无定形粉末,具有扬尘性,应避免吸入


-
拓展:在常温下,纯品过氧化钠为白色,但一般见到的过氧化钠呈淡黄色(混有超氧化钠的缘故
-
原理:超氧化钠含有超氧根离子 (带有自由基),对蓝紫区可见光有特殊吸收效果,少量混入即可使过氧化钠整体显淡黄色
9、催化剂不仅参与反应,其加入还可以变化反应进行的方向:
-
KClO3 热分解:
-
加入MnO2 :
10、铝不仅可置换活泼金属,还可以置换SiO2:
11、KNO3 也可分解,来自于硝酸盐特有的暴脾气:
12、高中所学习的硅酸其实为偏硅酸,对,就是矿泉水里面的那个东东
13、H2S 中混有HCl气体,可以通过盛有饱和NaHS溶液的洗气瓶除去(其他也是类似,通过饱和的元素目标价态的酸式盐溶液即可除去)
14、Al, Fe在浓硫酸中钝化,分别生成Al2O3 ,Fe3O4-γ-Fe2O3(尖晶石相) 。没错,四氧化三铁实际上难溶于浓(纯)硫酸,每天只有数纳米的反应(文献:Potter, E. C. 等 (1969). Passivity and Anodic Protection. CORROSION, 25(6), 233.等)
15、续上,Cu在稀硝酸中不钝化,Mg在浓硝酸中钝化(均为常温)
- 这里就要说说啦,也许你去 YouTube 看一些化学博主做铜和浓硝酸的反应,看现象似乎也出现了钝化,这是因为 TA使用的是浓度更高的发烟硝酸,生成的硝酸铜晶体附着在铜表面,由于其在极高浓度硝酸中溶解度降低,阻碍了酸液与金属的接触,因此加少量水就可继续反应
16、另一种可维持Fe(OH)2 长时间存在的装置图(汽油可换成苯,两者密度均小于水;图片源自Nano Banana Pro,谷歌👍):
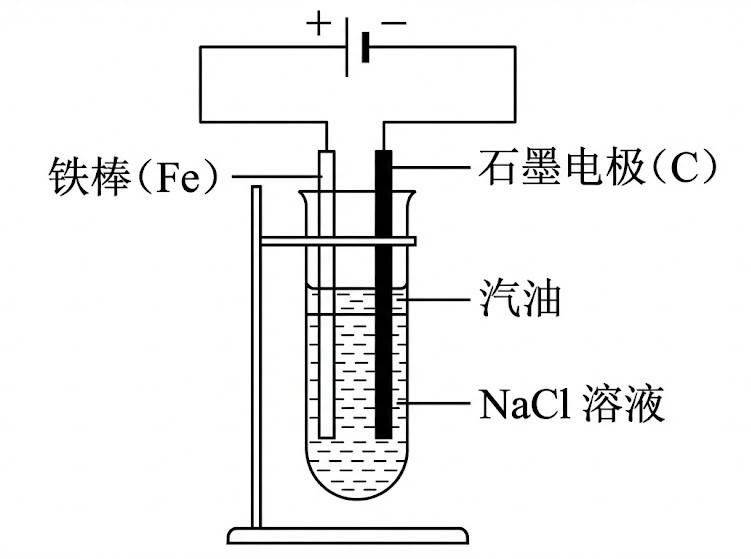
- 原理:

17、★★ 常见的与水混溶的物质:
- 全部都是因为氢键!
18、拟卤素的氧化性顺序:
19、存在反应:
20、对于 :

- 这让人想起:Na2S溶液能溶解硫生成多硫化钠(Na2Sx),这个是因为能够进攻 环状分子,导致硫环断裂,硫原子不断插入到原有的硫离子或多硫根离子中使其溶解;而Mg(OH)2能溶于NH4Cl原理又不一样,是因为沉淀溶解平衡和相互促进水解
- 都说到这了再多提一嘴,溶解当然也可以是配位,比如AgCl溶于氨水(AgI就不行了),又或:
21、★★ 存在以下神奇的反应:
- 这个反应高炉炼铁中非常重要,用来解释为什么CO在某些温度区间既能还原FeO,又会被FeO氧化,形成动态平衡
- 固体酒精:乙醇 + 醋酸钙溶液 → 形成凝胶(醋酸钙在乙醇中形成网状结构包裹乙醇分子)不要跟 混淆(这种物质的存在说明CaCl2 不能用于干燥乙醇)
22、★★ 与Mg在CO2 中燃烧不同,Mg在SO2 中燃烧,可能会产生 MgO, S, MgS中的多种产物
元素周期律类内容:
1、Fe, Au最外层均只有2电子,但均可形成三价离子。值得注意的是,Fe(III)比Fe(II)更稳定
2、稀有气体定位法:2/10/18/36/54/86/118
-
如51号元素锑(Sb):36<51<54,用51-36(更小的数字)=15
-
3-10为副族IIIB-VIII,8,9,10为VIII
-
11-12为IB IIB
-
1-2为IA IIA
-
13-17为 IIIA-VIIA
-
人造元素11x就在x族
3、★★★ 某一周期IIA族元素的原子序数为 ,则同周期的IIIA族的元素原子序数为?
- 显然成立;若考虑长周期,副族和VIII族共十列,所以也可为 ;若考虑镧系/锕系(各系内共15元素,两系在周期表中各占一个格子),则为
4、门捷列夫在编制周期表时按照r 排序,现代周期表按照质子数排序,故会出现后面元素相对原子质量大于前面元素的情况
5、★★ 过渡元素全部属于副族(×) 这个得看老师怎么讲,若认为VIII族不属于副族则答案为前面的
6、过渡元素普遍具有高熔点和独特的催化性能,可制催化剂
- 原理:副族元素大多具有神奇的电子排布,如Pd(钯)元素,其5s轨道完全空置(5s⁰),全部46个电子都挤进了前四层,4d亚层达到全充满;4d¹⁰结构虽然稳定,但在表面或配位环境下容易失去/得到电子,特别适合做加氢、偶联反应(如Suzuki、Heck反应)的催化剂;钯的吸氢能力也是此缘故
7、★★ 核素不一定是同种元素的原子,如H-3与O-18,它们互为核素
8、★★★ 原子结构示意图画法(主族):周期数=电子层数;主族元素序数=最外层电子数
- 举例:38(IIA 5P): 2/8/18/8/2;49(IIIA 5P):2/8/18/18/3
9、★ 臭氧是极性分子
-
为什么?臭氧不是平面分子,而是弯曲的 (被谁掰弯了?),键角约为116.8°,其极性主要来源于中心氧原子的孤对电子产生的偶极矩,它无法抵消,因而产生极性。下图一为臭氧结构式;图二为共振式(图片不显示就去Wiki镜像站看)
-


10、CH4 BH3 SiH4 中心原子价态分别为:-4, +3, +4
-
要注意:前者C +2价,N -3价;后者S -2价 C+4价 N -3价;故SCN-不能被氧化为CO2,只是单纯的转化
-
都说到化合价了,那就扯扯一个类似的问题:电子式
-
★★★ 电子式不一定要正负电荷交替排布(如氢氰酸 HCN)(许多教辅都是错的!),而是按照实际分子结构排布的 ( 那我又不知道分子结构长啥样,咋画捏 )很简单! 按照化合价来画,电负性(目前可以理解为非金属性)强的原子从共用电子对中降价,电负性弱的原子则升价
-
那就再送个公式吧,辅助你判断和验证电子式:
-
举例: 分子:饱和:N需要8,3H需要6,总共 14(单位:);实际:N有5,3H有3,总共 8 ∴共用电子对数:1/2(14-8)=3对,符合实际
11、 为空间分子
12、★★ 电子式表示物质的形成过程时应打箭头而不是等号
13、硫单质可以以单质形式存在于自然界中(火山口);卤素即便是I2也不可以
- 再说说碘:单质碘微溶于水,1 克碘在 20℃时溶于 3450 毫升水中,在 50℃时溶于 1280 毫升水中;碘的极性溶液(例如水溶液)是棕色的,显示溶剂充当了路易斯碱,生成电荷转移配合物;而非极性溶液则呈现紫色,也就是碘原本的颜色。
14、范德华力:结构相同的分子,r ,F
15、水结冰时密度减小,与氢键的方向性,饱和性有关
-
氢键个数的确定:①孤电子对个数(未与其他原子共用的电子对叫孤电子对)②氢原子个数 ①②中取较小值即为该分子中氢键个数
-
如NH3分子,①(1)②(3) 取较小值为1,故一个NH3中只有一氢键
16、★★ 晶体SiO2, SiC, Si3N4, C, S单质, P, Si 均由原子构成,因而融化时并不用克服分子间作用力
17、★ 容量瓶用蒸馏水洗净后,再用待配溶液润洗 (×)用蒸馏水洗净即可,反正最后都是要加水定容的,加入待配溶液会使得 偏高
- 核外电子层数越多,原子半径越大(×)如Li和Cl,分别为152pm和99pm(Cl是第三周期半径唯一小于100pm的元素)
18、★★ 常温常压下,32g 的混合气体所含的原子数为____
- 混合气体中只含氧原子,此为突破口。A AAA

